Коллоквиум по биохимии человека № 5.
1.
При сепсисе,
травме и других метаболических стрессах распад белков становится выше синтеза
(отрицательный азотистый баланс). При этом необходимо повысить количество
вводимого белка до 1,3-1,5 г/кг/день, несмотря на то, что в терминальном
состоянии, например, вследствие почечной
или печеночной недостаточности, поступление белков следовало бы ограничить.
2.
Азотистый баланс
– разница между поступающим азотом в форме белка и его выведением в форме
неусвоенного белка кишечником и мочевины почками.
При недостаточном или неполноценном белковом питании у
человека развивается отрицательный азотный баланс, т.к. поступающего белка
недостаточно для возмещения потерь выводимого кишечником и почками азота.
Поступление белков с пищей можно считать достаточным, если они компенсируют
потери (т.е. наблюдается равновесный азотистый баланс). Для взрослых суточная
доза азота около 0,8 г/кг/день.
3.
Незаменимые
АК: арг, вал, гис, иле, лей, лиз, мет, тре, три, фен. Арг и гис частично заменимы
(незаменимы для детей). Данные АК называются незаменимыми, т.к. в организме не
синтезируются углеродные скелеты этих АК и невозможно их образование с помощью реакций
трансаминирования. Последствия недостаточности незаменимых АК в пище:
отрицательный азотистый баланс, остановка роста и истощение, нарушения со
стороны НС, неполное усвоение других АК.
Коэффициент
изнашивания – количество азота,
теряемое человеком, находящимся на безбелковой диете (примерно 20 г белка в
сутки).
4.
Белки в желудке
перевариваются до АК, которые затем абсорбируются клетками кишечника и попадают в портальную
систему. Гидролиз белков (протеолиз) обеспечивается:
1)
НСl – секретируется обкладочными
кл слизистой желудка, функции:
а) понижает рН химуса б) денатурирует белки, вызывает
их набухание в) создает оптимальный рН для действия пепсина г) инициирует
ограниченный протеолиз пепсиногена д) бактерицидные свойства
2)
гастрин – гормон,
секретируемый в ответ на поступление химуса в желудок, стимулирует секрецию НСl обкладочными кл и секреция пепсиногена главными
клетками.
3)
пепсиноген –
профермент пепсина, гидролизует внутренние пептидные связи в пищевых белках
4)
пепсин –
преимущественно гидролизует пептидные связи, образованные ароматическими
группами ароматических и больших алифатических АК с образованием больших
пептидных фрагментов.
5)
ренин – в
желудочном соке грудных детей расщепляет белок молока – казеин.
5.
Оценка
кислотообразующей функций желудка имеет большое значение при диагностике
язвенной болезни, гастрита, злокачественных новообразований и др.
Общую кислотность желудочного сока в основном определяют:
а) свободная НCl – это НСl, которая
выделяется обкладочными клетками в чистом виде (20-40 ммоль/л)
б) связанная с белками НCl
в) кислые фосфаты
г) органические кислоты.
Содержание в норме 40-60 ммоль/л у взрослых, 2,8
ммоль/л у детей.
Принцип определение: титрование желудочного сока с помощью р-ра NaOH в присутствии фенолфталеина и последующий расчет общей
кислотности.
6.
Определение
содержания свободной соляной кислоты в желудочном соке: отсасывают содержимое
желудка с помощью зонда, затем энтерально (пробный завтрак) или парэнтерально
(гистамин) стимулируют секрецию HCl, вновь
отсасывают желудочный сок и титруют его р-ром NaOH с индикатором до изменения окраски. Затем рассчитывают
свободную кислотность. В норме она равна у взрослых 20-40 ммоль/л, у детей 0,5
ммоль/л.
7.
Эндопептидазы
– расщепляют пептидные связи внутри целой молекулы белка. Работают
при оптимальных рН и концентрации электролитов. Синтезируются в виде
неактивных проферментов, затем активируются путем ограниченного протеолиза.
Каждая эндопептидаза специфична по отношению к определенным пептидным связям,
продукт действия одного фермента может быть субстратом для другого.
Основные
эндопептидазы желудка и поджелудочной железы:
1)
пепсин – гидролиз пептидных
связей, образованных карбоксильными группами ароматических и больших
алифатических АК с образованием больших пептидных фрагментов.
2)
трипсин –
гидролизует пептидные связи, образованные карбоксильными группами основных АК – лиз и
арг.
3)
химотрипсин –
гидролизует пептидные связи, образованные карбоксильными группами ароматических
АК (фен, тир, три)
4)
эластаза –
гидролизует пептидные связи, образованные карбоксильными группами маленьких
алифатических АК (гли, ала, сер)
8.
Протеазы ЖКТ
активируются по механизму ограниченного протеолиза - избирательного гидролиза
одной или нескольких пептидных связей в молекуле белка с изменением
функциональной активности последнего.
Ограниченный П. имеет первостепенное значение для регуляции обмена
веществ в организме:
1)
образование и
инактивация ферментов, гормонов и других БАВ,
контроль активности основных биорегуляторов (пепсиноген ® пепсин, ПОМК ® АКТГ, проинсулин ® инсулин).
2)
образовании
ферментов, участвующих в свертывании крови и фибринолизе
3)
активация системы комплемента
4)
активация ренин-ангиотензинной и калликреин-кининовой
систем
5)
является одним из
важнейших механизмов репродукции
Ограниченный П. представляет собой один из основных механизмов
посттрансляционной модификации — процессинга белков.
9.
Экзопептидазы –
удаляют АК последовательно от N- или C-конца белковой молекулы.
а) Карбоксипептидазы (вырабатываются в поджелудочной
железе): карбоксипептидаза А – отщепляет нейтральные
АК с С-конца пептида, карбоксипептидаза В – основные АК с С-конца пептида.
б) Аминопептидазы (вырабатываются на границе тощей и
подвздошной кишки): аланинаминопептидазы (отщепляют
ала с N-конца), лейцинаминопептидазы (отщепляют все остальные АК с N-конца).
10. Гниение белков – совокупность превращений белков, вызванные
деятельностью микроорганизмов кишечника. При гниении образуется ряд токсических
продуктов распада: фенол, крезол, индол, скатол, сероводород, меркаптаны.
Данные продукты попадают в портальную систему и обезвреживаются в печени путем конъюгации
с глюкуроновой кислотой или с другими
веществами с образованием нетоксичных и растворимых соединений –
эфироглюкуроновых парных кислот.
11. Повышение активности аспарагиновой или аланиновой
аминотрансфераз в крови позволяет
распознавать патологические состояния, сопровождающиеся некрозом тканей, что и
используется для диагностики ряда заболеваний, контроля за
их течением, прогноза в будущем (пример: инфаркт миокарда, гепатит, рак печени,
мышечная дистрофия).
12. Диагностическое значение
определения активности аминотрансфераз в сыворотке крови:
а) увеличенный уровень может свидетельствовать о:
инфаркте миокарда, гепатите, алкогольном повреждении печени, раке печени,
мышечной дистрофии печени.
б)
сниженный уровень – о пищевой недостаточности пиридоксина, при беременности,
состоянии после гемодиализа.
Например,
при инфаркте миокарда активность АсАТ в крови
резко возрастает (в 5—10 раз по сравнению с нормой) через 4—6 ч
после начала заболевания, а затем постепенно снижается, достигая нормы примерно
через 5 дней. Повторное повышение активности АсАТ
в крови говорит о продолжающемся процессе некротического распада ткани
миокарда.
В
клетках сердечной мышцы (миокарда) содержится гораздо больше АсТ, чем АлТ, а в клетках печени
- наоборот: АлТ намного больше, чем АсТ. Поэтому ПРИ ИНФАРКТЕ МИОКАРДА АКТИВНОСТЬ АСТ в крови БУДЕТ ЗНАЧИТЕЛЬНО ВЫШЕ, ЧЕМ
АЛТ, А ПРИ ВИРУСНОМ ГЕПАТИТЕ АКТИВНОСТЬ АЛТ
БУДЕТ ВЫШЕ, ЧЕМ АСТ.
13.
Аланинаминотрансферазы в мышцах обеспечивают удаление
азота АК при их усиленном катаболизме. При повреждении мышц уровень АлАТ и АсАТ
увеличивается, что может служить дополнительным диагностическим критерием. См.
вопрос 11 и 12.
14.
Повышенное содержание в крови АлАТ может свидетельствовать о
некротических процессах в тканях (вопрос 12)
|
|
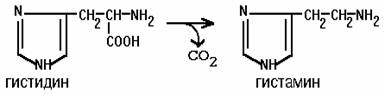
15.
Аллергические реакции нередко сопровождаются падением АД, т.к.
гистамин, выделяемый тучными кл, является вазодилятатором.
Образование гистамина из гистидина катализируется гистидиндекарбоксилазой.
|
|
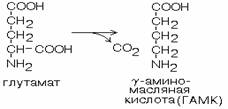
16. Реакция образования ГАМК катализируется глутаматдекарбоксилазой в кл серого вещества головного
мозга:
ГАМК является медиатором тормозных импульсов в
нервной системе. ГАМК и ее аналоги применяются в медицине как нейротропные средства для лечения эпилепсии и других
заболеваний.
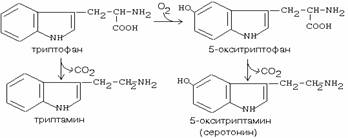
17. Пути синтеза серотонина (катализируется декарбоксилазой ароматических АК):
Роль
гистамина:
1) участник аллергических реакций 2) сильный вазодилятатор
3) расширяет капилляры и увеличивает сосудистую проницаемость 4) понижает
артериальное давление 5) повышает тонус (спазм) гладких мышц (бронхи) 6)
усиливает секрецию желудочного сока
Роль
серотонина:
1) сужает сосуды 2) регулирует свертывание крови 3) обладает антиаллергическим
действием.
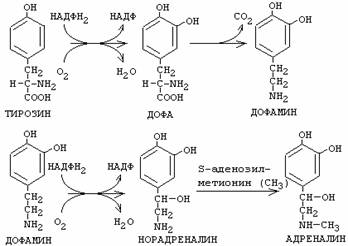
18.
Реакция синтеза дофамина (катализируется декарбоксилазой
ароматических АК) и его дальнейшее использование.
|
|
Роль
дофамина:
1) является предшественником
катехоламинов
2) нейромедиатор
3) метил-ДОФА – сильный ингибитор декарбоксилазы ароматических АК.
19.
Глутаматдегидрогеназа – играет ключевую роль в обмене АК:
Глутамат-ДГ - никотинамидная, отнимаемые протоны и электроны не передаются сразу
на кислород, а транспортируются по полной цепи МтО с
образованием воды и параллельным образованием трех молекул АТФ. Регуляторным
ферментом - ингибируется избытком АТФ, и активируется избытком АДФ.
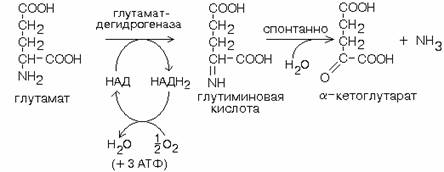
20.
Глутаматдегидрогеназная реакция (с коферментом НАДФ) – в обратном направлении:
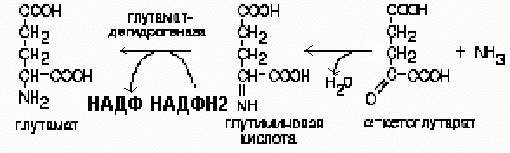
21.
Роль непрямого дезаминирования АК:
1)
Обеспечивает образование новых АК из числа заменимых.
2)
Образование необходимых клетке кетокислот из заменимых АК
3) Обеспечивают
синтез мочевины
4)
Главный путь удаления азота у АК при их интенсивном катаболизме
Суть
процесса: перенос аминогруппы одной АК на a-кетокислоту с образованием другой АК и другой a-кетокислоты.
22.
Реакции образования новых АК:
1)
переаминирование (трансаминирование)
2)
прямое гидролитическое дезаминирование (асн ® асп)
3)
аминирование (глу ® глн)
4) w-декарбоксилирование (асп ® ала)
23.
Аммиак может накапливаться в клетках и при участии митохондриальной глутаматдегидрогеназы активировать восстановительное
дезаминирование a-кетоглутаровой кислоты, элиминируя ее тем самым из цикла трикарбоновых кислот, что
ведет к угнетению тканевого дыхания и накоплению кетоновых тел. Интоксикация
аммиаком раньше всего проявляется симптомами угнетения ц.н.с.,
в тяжелых случаях может развиться кома.
24.
Пути обезвреживания аммиака в организме и в клетке:
а)
временное связывание – в тканях, интенсивно продуцирующих аммиак – в нервной и
мышечной:
1) связывание NH3 с глутаминовой, реже аспарагиновой кислотами с образованием глн и асн
2) аминирование остатков глу и
асп в составе белков
3) восстановительное аминирование a-кетоглутарата в глутамат, который в реакции
трансаминирования с ПВК образует ала – резервный и транспортный источник
аммиака.
б)
общее (конечное) обезвреживание
1) выведение в виде солей
аммония
2) синтез мочевины
25.
У детей незаменимыми являются заменимые у взрослых АК:
гис и арг.
Роль
гис:
является предшественником важного биоамина – гистамина.
Роль
арг:
1)
участвует в синтезе креатина в почках
2)
в составе белков аргинин как полярная положительно заряженная аминокислота
участвует в образовании ионных связей и в формировании
гидратной оболочки белков
3)
участник орнитинового цикла мочеобразования
26.
Синтез мочевины – главный путь обезвреживания аммиака в печени.
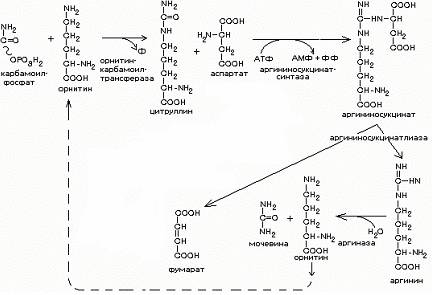
27.
Основными транспортными формами аммиака в печень и почки является
ала и глн.
29.
В случае чувствительности при некоторых формах лейкоза опухолевых клеток к
недостатку аспарагина для лечения можно использовать АсАТ (аспарагиновую
аминотрансферазу).
30.
Другие органы, кроме почек и печени также могут обезвреживать аммиак (см.
вопрос 24 – местные механизмы)
31.
Значение определения мочевины в крови в клинической практике:
а) повышение
уровня мочевины в крови может свидетельствовать о 1) нарушении функции почек
(хронической и острой почечной недостаточности), 2) внепочечные причины:
обезвоживание организма, усиленный распад белков (острая желтая дистрофия
печени, злокачественные опухоли и др.).
б)
понижение концентрации мочевины в крови: 1) повышенная скорость клубочковой фильтрации
(у беременных молодых женщин, при нагрузке чрезмерным объемом внутривенных
вливаний) 2) патологическое изменении значительной части паренхимы печени 3)
недостаточности белка в питании, продолжительном голодании 4) врожденное
нарушение нормального протекания цикла мочевины (у детей).
32.
Содержание мочевины в крови в норме 2,5-8,3 ммоль/л. Причины повышения – см.
выше. При уремии следует ограничить поступление белков с пищей. При этом, предпочтение отдают белковым продуктам, в которых
представлены в правильном соотношении все эссенциальные аминокислоты и
ограничивают при этом растительный белок, чтобы нормализовать и поддержать
азотистый баланс и нейтрализовать симптоматику отравления. В случае проведения
гемодиализа поступление белков ограничивать не стоит, возможно
даже увеличение количества вводимых белков выше нормы.
33.
Возможные пути использования безазотистых остатков АК - кетокислот в кл:
1)
источник энергии (a-кетоглутаровая
к-та, ЩУК ® ЦТК)
2)
синтез новых АК
3)
образование кетогенных тел
4)
обезвреживание аммиака (глутаматдегидрогеназная реакция)
Кетокислоты
обеспечивают интеграцию метаболизма АК, углеводов и липидов.
34.
АК могут служить источником энергии в клетке. Гликогенные АК могут превращаться
в ПВК, a-кетоглутаровую к-ту, ЩУК,
сукцинил-КоА, фумаровую к-ту ® ЦТК ® энергия. Кетогенные АК превращаются в ацетил- или ацетоацетил-КоА и идут на синтез кетонных тел ® энергия.
35.
Избыток белков ® образование избытка гликогенных и кетогенных АК ® повышение содержания ПВК, ацетил-КоА,
ацетоацетил-КоА ® синтез ВЖК и кетоновых тел
и их запасание
36.
Глу – гликогенная АК:
а)
реакция трансаминирования глу + ПВК ® a-КГ + ала
б)
реакции ЦТК: a-КГ ® сукцинил~КоА ® сукцинат ® фумарат ® малат ® ЩУК
б)
реакции глюконеогенеза: ЩУК® ФЕПВК ® ФР-1,6-ФФ ® ФР-6-Ф ® гл-6-ф ® гл
37.
Из ала можно синтезировать гл:
1)
реакция трансаминирования: ала + a-КГ®ПВК + гл
2)
реакции глюконеогенеза: ПВК®ЩУК ® ФЕПВК ® ФР-1,6-ФФ ® ФР-6-Ф ® гл-6-ф ® гл
38.
Проявления недостаточности ферментов, участвующих в обмене фенилаланина и
тирозина:
1)
фенилкетонурия - нарушен синтез фенилаланин-гидроксилазы, поэтому фенилаланин
превращается в фенилпируват, который оказывает токсическое воздействие на
развитие некоторых отделов головного мозга.
2)
альбинизм - нарушен синтез ферментов, превращающих ДОФА в ДОФА-хром,
поэтому нарушается синтез меланинов.
3)
алкаптонурия - нарушен синтез диоксигеназы гомогентизиновой кислоты, она
выделяется с мочой, моча приобретает черный цвет.
4) кретинизм - нарушен синтез йодиназы, что приводит к
нарушению синтеза йодсодержащих гормонов щитовидной железы.
5)
может быть нарушен синтез фермента тирозиназы,
который катализирует превращение тирозина в ДОФА, следовательно
будет нарушаться синтез гормонов мозгового слоя надпочечников и меланина.
Из всех этих заболеваний в
настоящее время удается лечить фенилкетонурию (из рациона ребенка исключают
фенилаланин и увеличивают в пище количество тирозина). Если ребенка держать на этой диете до 6-7
лет, тогда не возникает умственная
отсталость, т.к. к 6-7 годам успевают
развиться отделы головного мозга, развитие которых задерживается при избытке в
ткани мозга фенилпирувата.
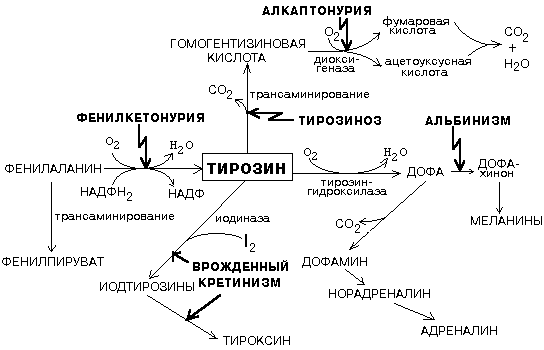
39.
Остаточный азот сыворотки крови –
азотсодержащие небелковые вещества (промежуточные или конечные продукты обмена
простых и сложных белков) – мочевина, мочевая кислота, креатин, креатинин,
аммиак, индикан, билирубин и т.д. Азот этих веществ называют остаточным, т.к.
он остается в фильтрате после осаждения белков.
Основная
часть остаточного азота крови – азот мочевины (50%), азот АК (25%) и азот
других азотсодержащих соединений. Норма остаточного азота крови для взрослых
14,3-25,0 ммоль/л. Остаточный азот определяют в безбелковом фильтрате после
осаждения белков с последующей минерализацием
фильтрата концентрированной серной кислотой. При этом образуется сульфат
аммония, который образует с реактивом Несслера соединение желто-оранжевого
цвета. Интенсивность окрашивания пропорциональна содержанию азота. Значение
метода: диагностика поражения почек (исследование выделительной функции) и
мочевинообразовательной функции печени.
40.
Нуклеотиды – мономеры нуклеиновых
кислот – состоят из:
1)
азотистого основания (у всех нуклеиновых кислот)
2)
пентозы (рибозы у РНК или дезоксирибозы у ДНК)
3)
остатка фосфорной кислоты
Азотистое
основание + пентоза = нуклеозид.
Свойства
нуклеотидов: 1) отрицательно заряжены (за счет фосфатных групп) 2) циклические
соединения 3) гидрофобны 4) поглощают свет при 260 нм (УФ область).
Функции
нуклеотидов:
1) структурная –
мономеры нуклеиновых кислот, входят в состав коферментов
2) энергетическая
(АТФ - это универсальный аккумулятор энергии, энергия УТФ используется
для синтеза гликогена, ЦТФ - для синтеза липидов, ГТФ - для движения рибосом в
ходе трансляции (биосинтез белка) и передачи гормонального сигнала (G-белок)
3) регуляторная
-
аллостерические эффекторы многих ключевых ферментов, цАМФ и цГМФ являются
посредниками в передаче гормонального сигнала при действии многих гормонов на клетку и активаторами протеинкиназы
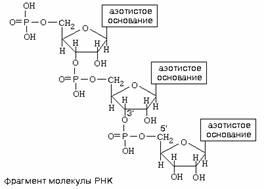
41. Первичная
структура НК – линейная последовательность нуклеотидов в одной цепи.
Нуклеотиды связываются через остатки фосфорной кислоты с помощью 3’,5’-фосфодиэфирных
связей.
42. Вторичная
структура ДНК – пространственная ориентация полинуклеотидных цепей в ее
молекуле. Представляет собой двойную правозакрученную спираль диаметром 1,8-2,0
нм. Полинуклеотидные цепи антипараллельны и комплементарны. Двойную спираль стабилизируют:
1) водородные связи между азотистыми основаниями
2) Вандерваальсовы силы
между азотистыми основаниями
3) гидрофобные взаимодействия
43. Принцип в основе формирования двойной спирали в
молекуле ДНК – комплементарность (А-Т (две водородные связи), Г-Ц(три водородные связи).
В РНК такой принцип не реализуется, т.к. она одноцепочечная, в гибридах типа ДНК-РНК комплементарность
реализуется в процессе транскрипции, при этом Г соответствует Ц, а А – У.
44. Третичная
структура ДНК и тРНК необходима для компактности молекул в ядре (ДНК) и в
цитоплазме (тРНК). Третичная структура тРНК формируется самостоятельно (в виде
двойной буквы Г), а ДНК – в результате связи с белками с образованием
нуклеопротеинов 4-х уровней упаковки: нуклеосомный, соленоидный, петлевой, уровень метафазной хромосомы.
45. Нуклеосома – глобула (октамер),
состоящая из белкового ядра (из 8 молекул-гистонов, Н2А, Н2В, Н3, Н4 – по две молекулы каждого вида), вокруг которого ДНК
делает 1,5-2 оборота. При этом длина накрученного фрагмента ДНК порядка 50 нм,
а компактизация составляет в 5-7 раз по сравнению с исходной.
Гистоновые белки
обладают положительным зарядом в связи с большим содержанием основных АК – арг
и лиз, связь между белками и ДНК – ионная.
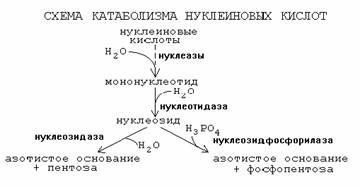
46.
Нуклеопротеины под действием желудочного сока (НCl)
распадаются на белки и нуклеиновые кислоты. Белки катаболизируются
до АК, затем всасываются, НК – до нуклеозидов, которые также всасываются. В кл
с ними происходит распад либо до АО и пентозы, либо до
АО и фосфопентозы:
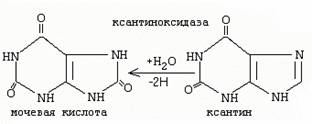
47.
При гиперурикемии повышается образование мочевой
кислоты под действием ксантиноксидазы:
48.
Причины повышения уровня мочевой кислоты
в крови:
1)
нечувствительность к регуляторам ферментов синтеза пуринов de novo
2)
снижение активности ферментов реутилизации пуринов
3)
почечная патология
4)
нехватка витамина B9
Последствия:
гиперурикемия и подагра (накопление
кристаллов мочевой кислоты в суставах).
49.
Синтез пуриновых нуклеотидов путем:
а) повторного использования готовых азотистых оснований (характерно для
размножающихся тканей) б) de novo из низкомолекулярных
предшественников (источники N – аспартат,
глицин, глутамин, источники С – СО2,
глицин, двухуглеродные фрагменты метенил-ТГФК
и формил-ТГФК).
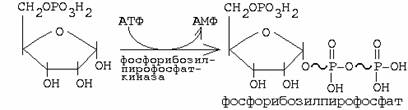
ФРПФ + глутамин -------> глутамат + ФФ +
фосфорибозиламин (катализируется ключевым
ферментом фосфорибозиламидотрансферазой)
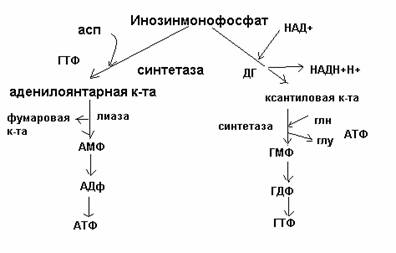
Основные
промежуточные продукты: фосфорибозиламин, инозинмонофосфат, аденилоянтарная,
ксантиловая кислоты.
50.
Синтез пиримидиновых нуклеотидов.
Сначала
образуется циклическая структура
пиримидинового азотистого основания, и только затем присоединяется
рибозо-5-фосфат. Источники атомов – СО2,
аспартат, глутамин.
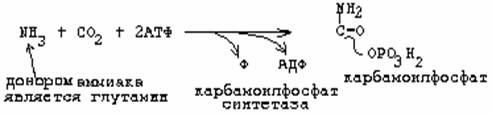
Карбамоилфосфатсинтетаза
II является ключевым ферментом.
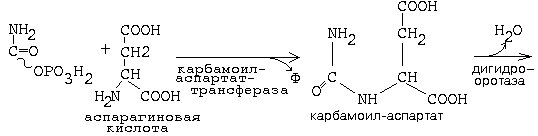
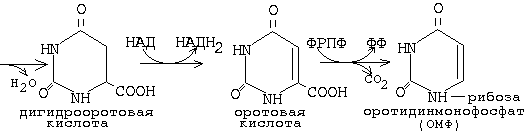
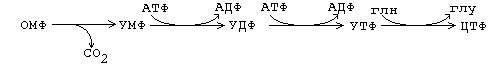
Основные
промежуточные продукты: карбомоилфосфат, оротовая к-та, дигидрооротовая к-та.
51. Дефицит
фолиевой кислоты (витамина В9) может привести к
нарушению синтеза пуринов и пиримидинов ® нарушение синтеза НК, процессов
репарации.
52. Реакция,
ведущая к образование карбамоилфосфата, общая для
синтеза пиримидиновых оснований и мочевины:
а) для
пиримидинов (карбамоилфосфатсинтетаза II):

б)
для мочевины:
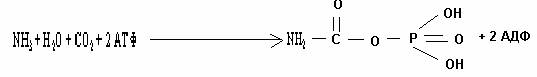
53.
Дезоксирибонуклеотиды образуются из
рибонуклеотидов путем восстановления рибозного остатка при участии
специфической фосфатной системы и фермента рибонуклеозидредуктазы. Донором
ионов водорода в этой реакции служит тиоредоксин – низкомолекулярный белок, содержащий
SH-группы.
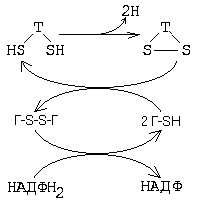
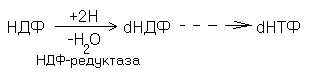
Тиоредоксин
получает два атома водорода от
трипептида глутатиона,
переходящего при этом в окисленную форму. Последующее восстановление
окисленного глутатиона происходит с помощью фермента глутатионредуктазы, использующей для этого НАДФН2.
54.
Репликация – процесс удвоения ДНК,
происходящий в S-фазу клеточного цикла. Полуконсервативный процесс.
Главный фермент – ДНК-полимераза, ведущая синтез дочерней цепи по принципам
комплементарности, антипараллельности, в одном направлении от 5’ к 3’ концу.
Субстраты
для синтеза ДНК: нуклеозид-3-фосфаты: дАТФ, дГТФ, дЦТФ, дТТФ. ДНК-полимераза
также требует кроме субстратов, ионы магния и праймер. Праймер – затравочный
олигонуклеотид, синтезируемый праймазой.
Репликация
начинается в местах повышенной концентрации пар А-Т.
Фермент хеликаза раскручивает двойную спираль, фермент топоизомераза снимает
напряжение в области репликативной вилки и предотвращает обратное скручивание,
ДНК-полимераза I удаляет остатки праймера. Терминация репликации наступает у
человека после 8-9 часов, при этом ДНК-лигаза сшивает
отдельные фрагменты Оказаки.
55.
Репарация – внутриклеточный процесс
восстановления поврежденной из-за неблагоприятных воздействий структуры ДНК.
Различают: а) дорепликативную б) репликативную
в) пострепликативную репарации. Прямая репарация –
химическая реакция, направленная на восстановление структуры поврежденного
нуклеотида, эксцизионная репарация – вырезание
поврежденного фрагмента с участием ряда ферментов:
1)
эндонуклеазы – узнает поврежденный участок и разрывает рядом с ним нить ДНК
2) экзонуклеазы – вырезает поврежденный участок
3)
ДНК-полимеразы – комплементарно достраивает фрагмент ДНК на месте разрушенного
4) лигаза – сшивает концы ресинтезированного
участка с основной нитью ДНК.
Роль
репарации: обеспечение постоянства генетического материала.
56.
Синтез и-РНК. – транскрипция –
переписывание информации с ДНК на и-РНК. Для эукариот
в этом процессе участвуют: РНК-полимераза I – синтезирует р-РНК, РНК-полимераза
II – синтезирует и-РНК, РНК-полимераза III – т-РНК. Субстраты синтеза: матрица,
рибонуклеозидтрифосфаты, праймер не требуется. Синтез идет антипараллельно, от
5’ к 3‘ концу. Вначале и-РНК образуется в виде предшественника – пре-и-РНК, затем идет кэпирование
– присоединение 7-метилгуанозина к 5’-концу полиаденилового
конца для защиты этого конца от нуклеаз, помогает присоединиться к рибосомам.
На 3’- конце идет полиаденилирование – для защиты от
нуклеаз, участвует в транспорте из ядра в цитоплазму.
57.
Единица транскрипции у эукариот
– транскриптон:
неинформативная зона (промотор) и информативная (структурные гены – экзоны –
информативны, интроны – нет + спейсеры – вставки, разделяющие структурные
гены). В отличие от прокариот
у эукариот работу транскриптона регулируют несколько
генов-репрессоров, а индукторами являются сложные молекулы (гормоны и т.д.),
часто требуется несколько индукторов – ступенчатый процесс. Образуемая
в процессе транскрипции и-РНК содержит неинформативные участки и подвергается
процессингу (вырезание неинформативных участков) и сплайсингу
(склеиванию оставшихся фрагментов).
58.
Обратная транскрипция – передача
генетической информации от и-РНК к ДНК с помощью
фермента обратной транскриптазы (ревертазы). В ходе этого процесса комплементарно синтезируется одна цепь ДНК на
основе и-РНК, а затем достраивается вторая цепь ДНК на основе первой.
Роль:
1) один из способов репарации ДНК 2) получение множественных копий ДНК 3)
передача генетической информации у ряда вирусов
59.
Генетический код – система записи генетической информации в ДНК (РНК) в виде определенной
последовательности нуклеотидов. Последовательность нуклеотидов определяет
последовательность включения АК в синтезируемый белок. 3 нуклеотида – триплет –
кодон – кодируют 1 АК. Совокупность триплетов и составляет генетический код.
Свойства
генетического кода:
1) триплетность
2)
вырожденность (избыточность – 1 АК кодируется несколькими триплетами)
3)
специфичность (1 кодон кодирует только 1 АК)
4) однонаправленность (от 5’ к 3’ концу)
5) неперекрываемость (один нуклеотид входит в состав только
одного кодона)
6)
универсальность (у всех живых организмов одинаковые АК
кодируются одинаковыми кодонами)
7)
отсутствие знаков препинания внутри гена.
60.
тРНК (10-15% от все РНК)
транспортирует АК к месту синтеза белка – на рибосомы. Имеет форму клеверного
листа, содержит два основных центра:
а)
антикодон – для связывания АК
б)
участок для прикрепления АК (5’ и 3‘
концы)
Нуклеотидная
цепь тРНК содержит всего 75—90 нуклеотидов. Особенностью тРНК является относительно высокое
содержание нуклеотидов, включающих минорные
азотистые основания. Т-РНК с помощью высокоспецифичных ферментов
аминоацил-тРНК-синтетаз присоединяют к себе ту или иную аминокислоту и
переносят ее на рибосому. Для одной и той же аминокислоты имеется несколько
тРНК, которые называют изоакцепторными.
Транспортная РНК в ходе синтеза полипептидной цепи белка
«узнает» специфическую аминоацил-тРНК-синтетазу, принимает от нее
активированную аминокислоту, присоединяется к иРНК на рибосоме и тем самым обеспечивает
строгую специфичность выбора и встраивания аминокислот в растущую молекулу
белка; после образования пептидной связи между доставленной аминокислотой и
уже построенной полипептидной цепью тРНК удерживает эту цепь на рибосоме.
61.
Аминоацил-тРНК-синтетаза – фермент, участвующий в
биосинтезе белка, отвечает за специфичность связывания АК с тРНК.
АК
+ АТФ ® ФФн
+ аминоацил-аденилат + тРНК ® АМФ + аминоацил-тРНК.
Известно
20 аминоацил-тРНК-синтетаз (по количеству L-АК). Содержит 4 участка:
для АК, для т-РНК, для воды, для АТФ. Правильность присоединения АК.
62.
Рекогниция – процесс узнавания тРНК своей АК, происходящий при помощи
фермента аминоацил-тРНК-синтетазы.
63.
Трансляция – синтез полипептида с
последовательностью АК, отвечающей последовательности триплетов нуклеотидов в
молекуле и-РНК. Этапы трансляции: 1) кодирование 2) рекогниция
3) собственно трансляция: инициация, элонгация, терминация.
Участники
трансляции: и-РНК, рибосомы, аминоацилтРНК,
активированные формы АК, ГТФ, факторы инициации, элонгации, терминации.
Перед началом синтеза белка рибосомы диссоциированы. На этапе инициации к
малой субъединицы рибосомы 3’ концом присоединяется и-РНК. К первому
инициирующему кодону присоединяется 1 аминоацил-тРНК,
несущая метионин. Затем присоединяется к образованному
комплексу большая субъединица рибосомы с затратой ГТФ – образование
инициирующего комплекса. В рибосоме образуется два центра – аминоацильный
и пептидильный. В свободный
А-центра поступает следующая аминоацил-тРНК ®
фермент пептидил трансфераза
образует пептидную связь между АК, дипептид остается в А-центре® транслоказа
перемещает рибосому на 1 кодон и-РНК ® дипептид при этом
оказывается в П-центре ® в освободившийся А-центр
поступает следующая АК.
Элонгация
заканчивается терминацией – наступает, когда в А-центр оказывается один из трех нонсенс-кодонов
(стоп-кодонов): УАА, УАГ, УГА. Они не соответствуют ни одной тРНК, распознаются
рилизинг-ферментами, которые вызывают отсоединение
синтезированного белка и диссоциацию рибосомы.
61.
Регуляция транскрипции у прокариот.
Единица
транскрипции прокариот – оперон,
состоит из 1) промотора – места первичного прикрепления РНК-полимеразы, 2)
оператора – включает и выключает экспрессию структурных генов 3) структурных
генов. На некотором расстоянии от оперона находится ген-регулятор, отвечающий
за синтез белка-репрессора, способного вступать в химическое взаимодействие
с геном-оператором и «выключать» его
работу.
Поступление
в кл индуктора ® индуктор+белок-репрессор ® освобождение гена-оператора ® РНК-полимераза присоединяется к промотору ® комплементарно со структурных генов
создается и-РНК ® трансляция и-РНК ® синтез фермента, разрушающего индуктор ® освобождение белка-репрессора ® присоединение его к оператору ® остановка трансляции.
65,67.
ПЦР – увеличение количества копий
ДНК, находящейся в биологическом материале в минимальных количествах. Этапы: 1)
денатурация ДНК (до 90°) 2) добавление
специфического праймера и охлаждение ДНК
(до 55°) (отжиг) 3) добавление
нуклеотидов (субстратов синтеза) и ДНК-полимеразы (фермента синтеза) 4)
повторение цикла. Позволяет за короткое время получить множество копий ДНК
(порядка 20 млн за 0,5 ч).
Применение: 1) диагностика вирусных и
бактериальных инфекций (ВИЧ, гепатит, хламидиоз) 2) генетическая диагностика
заболеваний 3) судебная медицина.
66.
Расшифровав нуклеотидную последовательность гена, можно установить последовательность АК в
кодируемом белке, однако следует помнить что ген содержит некодирующие последовательности –
интроны и спейсеры, которые удаляются в ходе процессинга и сплайсинга и не
отражаются в структуре конечного белка. Поэтому, чтобы достоверно установить
последовательность АК в белке, можно методами генетической
инженерии синтезировать белок, а затем подвергнуть его биохимическому
анализу (электрофорезу).
68.
Клонирование – получение большого
количества молекул, клеток, организмов – потомков одного предка. Для
клонирования бактериальных и вирусных генов необходимы носители генетической информации – плазмиды, ДНК (РНК) бактериофага,
нуклеоид, хромосомы дрожжей.
Этапы:
1) получение генетического материала 2)
включение гена в векторную молекулу, создание рекомбинантной ДНК 3)
введение рекДНК в кл хозяина 4) отбор трансформированных кл на селективных
средах.
Применение:
1) получение разнообразных вакцин и иммунологических диагностикумов 2) синтез
ряда БАВ: СТ, инсулин, эритропоэтин, интерфероны,
факторы свертывания крови 3) получение ферментов в промышленности 4) получение
относительно недорогого пищевого белка для животных и т.д.
69.
Вектор – природный ген определенного
микроорганизма с внедренным в него участком чужеродного гена. В качестве
векторов применяется: 1) плазмида – небольшая
кольцевидная молекула ДНК бактерий, реплицируемая независимо от нуклеоида 2) бактериофаг лямбда 3) хромосомы дрожжей 4) космидные векторы - гибрид фага лямбда и плазмиды.
70.
«Метод отпечатков пальцев» ДНК
используется для: 1) идентификации личности в судебной медицине 2) комплексной
диагностики наследственных заболеваний 3) поиске участков ДНК, отвечающих за
развитие патологии 4) установления отцовства.
В
основе метода – принцип гибридизации на основе комплементарности.
71.
Рестриктазы (рестриктационные
эндонуклеазы) – ферменты, узнающие специфическую последовательность
нуклеотидов и разрывающие в этом месте молекулу ДНК. Действуют в области
палиндромов ДНК – мест, где последовательность нуклеотидов одной цепи идентична
последовательности нуклеотидов другой цепи, прочитанной в обратном порядке. В
молекулярной биологии рестриктазы используют для
создания генетических векторов (внедрение гена в плазмиду
и т.п.)
72.
При проведении блот-анализа ДНК используют одноцепочечную
молекулу ДНК, комплементарную искомой и меченую
радиоактивным фосфором P32. Позволяет
диагностировать в геноме дефектные гены, установить наличие наследственных
заболеваний.
73.
Этапы постановки блот-анализа ДНК:
1)
экстракция ДНК
2)
разрезание ДНК рестриктазами
3)
разделение ДНК путем электрофореза в агарозном геле
4)
перенос ДНК на нитроцеллюлозу и денатурация ее щелочью
5)
блокирование пустых зон избытком ДНК
6)
обработка зондом и образование гибридов мишень-зонд
7)
отмывка несвязанного зонда и ауторадиография